CE认证是欧盟的产品安全认证,所有进入欧盟市场的医疗器械都必须进行医疗器械CE认证,医疗器械需要满足的CE指令有《有源植入性医疗器械指令》(AIMDD, 90/385/EEC)、《医疗器械指令》(MDD,93/42/EEC)和《体外诊断器械指令》(IVDD, 98/79/EC)。
CE认证是欧盟的产品安全认证,所有进入欧盟市场的医疗器械都必须进行医疗器械CE认证,医疗器械需要满足的CE指令有《有源植入性医疗器械指令》(AIMDD, 90/385/EEC)、《医疗器械指令》(MDD,93/42/EEC)和体外诊断器械指令(IVDD, 98/79/EC)。
认证项目 | CE认证 | 
|
认证周期 | 详情咨询 |
认证对象 | 企业与工厂等 |
认证费用 | 详情请咨询:18022213930 |
欧盟CE医疗器械安全认证标志
以下以取得CE认证为例说明:
产品要顺利通过CE认证,需要做好三方面的工作。
第一,收集与认证产品有关的欧盟技术法规和欧盟(EN)标准,通过消化、吸收、纳入企业产品标准。
第二,企业严格按照以上产品标准组织生产,也就是把上述技术法规和EN标准的要求,贯彻到企业产品的设计开发和生产制造的全过程。
第三,企业必须按照ISO9001+ISO13485标准建立和维护质量体系,并取得ISO9001+ISO13485认证。
获得CE标志的一般程序
国内的一些医疗器械厂家(特别是一些乡镇企业)对医疗器械指令不甚了解,不知如何着手申请CE标志。为此我们简单地介绍获得CE标志所需步骤如下:
步骤一、分析器械及特点,确定它是否在指令的范围内医疗器械的定义在指令中作了明确的规定,医疗器械,如一些、额温枪、核酸检测试剂盒、体温计、医用护目镜、呼吸机等。医疗器械指令范围的产品。
步骤二、确认适用的基本要求指令规定,任何医疗器械必须满足指令附录Ⅰ中所规定的预期用途,所以对制造商来说,首先要做的而且最重要的事情就是确认所有的适用于其产品的基本条件。
步骤三、确认任何有关的欧洲协调标准协调标准是由欧洲标准委员会(CEN)和欧洲电气技术委员会(CENELEC)制定的公布在欧盟官方杂志上的标准,对于某种医疗器械来说,可能有多种协调标准适用于它。因此在确认哪些协调标准适用于它。因此在确认哪些协调标准适用于某种产品时应十分仔细。
步骤四、确保产品满足基本要求或协调标准的要求并且使证据文件化·制造商应能提出充分的证据(如由公告机构或其他检测机构依据协调标准进行的检测等)来证明产品符合基本要求。
步骤五、产品分类根据指令附录Ⅸ的分类规则,医疗器械分成4类,即Ⅰ、ⅡA、ⅡB和Ⅲ类,不同类型的产品、其获得CE标志的途径(符合性评价程序)不同,因此对制造商来说,如何准确地确定其产品的类型,是十分关键的。
步骤六、确定相应的符合性评价程序对于Ⅱa、Ⅱb、Ⅲ类医疗器械的制造商来说,存在着如何选择符合评价程序途径的问题。主要的区别是选择型式试验的方式,还是选择质量体系的方式,这两种途径各有其特点。制造商应根据自己的实际情况选择最为适合的途径。
步骤七、选择公告机构对于Ⅱa、Ⅱb和Ⅲ类医疗器械,以及无菌的或具有测量功能的I类医疗器械,应选择一个公告机构并进行符合性评价程序。在欧盟官方杂志上公告的公告机构名单上,对每个公告机构可以从事的医疗器械认证以及可进行的符合性评价程序途径都有严格的规定,制造商在选择公告机构时,必须非常谨慎,避免造成不必要的损失。
步骤八、起草符合性声明并加贴CE标志可以说符合性声明是重要的文件。每一种器械必须包括医疗器械指令的附录中所描述的符合性声明。
证书的分类
有如下几种类型的CE证书:
(1)Declaration of conformity / Declaration of compliance《符合性声明书》,此证书属于自我声明书,不应由第三方机构中介或测试认证机构签发,因此,可以用欧盟格式的企业《符合性声明书》代替。
(2)Certificate of compliance / Certificate of compliance《符合性证书》,此为第三方机构=(中介或测试认证机构)颁发的符合性声明,必须附有测试报告等技术资料TCF,如果没有测试报告也可交由第三方机构办理。同时,企业也要签署《符合性声明书》。
(3)EC Attestation of conformity 《欧盟标准符合性证明书》,此为欧盟公告机构(Notified Body简写为NB)颁发的证书,按照欧盟法规,只有NB才有资格颁发EC Type的CEE声明,此证书可用作清关,为一次性证书
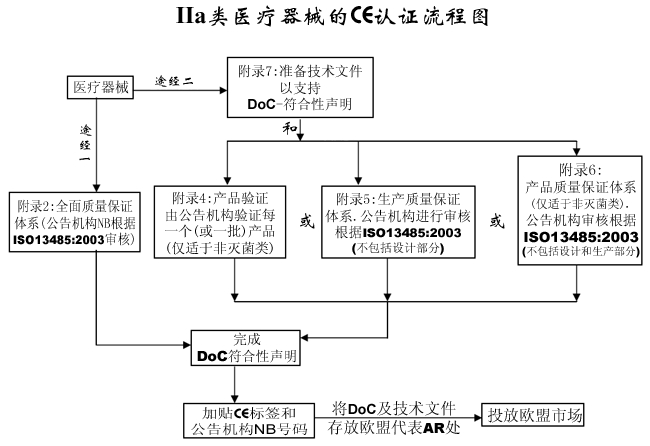
第Ⅰ类。第Ⅱa类、第Ⅱb类、第Ⅲ类产品要加贴CE标志,则必须由欧盟指定的验证机构验证。欧盟还规定,这几类产品获得CE认证的先决条件是制造厂需能过ISO9000+ISO13485质量体系认证,取得ISO9000+ISO13485质量体系认证证书,且证书的颁发单位应为欧盟认可的认证机构。ISO9000+ISO13485质量体系认证和CE认证可同时进行,但CE证书必须待ISO9000+ISO13485质量体系认证通过后,方可予以颁发。
按照欧盟对产品的分类伽玛刀属于第Ⅱb类,其CE认证程序和内容如下:
(1)企业向认证机构提出认证申请,并填写认证询价单交认证机构;
(2)认证机构向申请认证企业提出报价单,企业签字确认即完成合约;
(3)企业向认证机构提交ISO9000+ISO13485质量体系文件即质量手册和程序文件,供认证机构进行体系文件审核;质量体系审核前,企业应有至少三个月的质量体系运行记录,并完成1-2次内部质量体系审核。
(4)认证机构发出认证产品测试通知单给认证机构认可的实验室,实验室将对申请认证的产品进行低电压(LVD)测试和电磁兼容性(EMC)测试。测试中若出现不合格,由企业改下后重新测试,直到测试合格为止。测试结束,实验室出具试验报告。
(5)企业编写申请认证产品的技术文件档案(简称TCF文件)。上述试验报告也作为TCF文件内容之一。TCF文件是申请CE认证的制造商向CE认证机构提交的一份重要文件,它是认证机构审核发证的重要依据。编制TCF文件必须全部使用英文。

TCF文件包括七个方面的内容:
① 简介;
② 产品的规格叙述;
③ 设计之主要档案内容;
④ 风险分析及评估;
⑤ 测试报告及临床诊断资料;
⑥ 文件设计的管制;
⑦ 产品申请的声明宣言。
(6)认证机构对企业的ISO9000+ISO13485质量体系和TCF文件进行初审。初审后认证机构将指出质量体系和TCF文件中存在的问题,企业应据此完善质量体系和TCF文件。
(7)认证机构对企业的ISO9000+ISO13485质量体系和TCF文件进行正式审核。
(8)正式审核通过后,认证机构将与企业签订框架协议,明确取得CE证书后各方应遵循原则和产品使用CE标志的范围,以及用投诉的处理办法。然后颁发ISO9000+ISO13485质量体系认证证书和CE标志证书。
- 医疗器械CE认证-(MDD指令)适用范围 -
1.安全性(任何风险与器械提供的益处相比较,必须在可以接受的范围内,故亦称风险分析);
2.风险的可预防性或被消除性,至少应给予警告(报警系统或警戒报警系统);
3.性能符合性(产品的基本要求);
4.器械性能和安全的效期(器械的安全和性能必须在器械的使用寿命内得到保证。);
5.器械的储存和运输(应保证器械在合理的运输、储存条件下不受影响)。
提供的服务
欧盟公告机构为国内企业提供全面的医疗器械产品认证服务,以期企业能够满足欧盟CE要求,同时我们将充分利用我们国际化的平台,为医疗器械企业提供更加全面的服务。
我们采用不同的认证模式,为生产不同医疗器械产品的制造商提供认证服务,服务包括:
1.产品分类判定
2.企业技术文件协助
3.企业管理提携协助
4.产品测试
5.工厂审核(适用时)
6.CE证书颁发
欧盟公告机构背景1. 亚太总部位,为客户提供快捷、专业、值得信赖的服务;
2. 技术专家长期参与欧洲法规的研究和制定,数十年的产品及体系认证经验,为客户提供一站式解决方案;
3. 认证产品涉及各种不同类别的医疗器械,获证客户数超过300家;
4. 公开,公正的认证服务过程,确保客户全程监控。
技术文件
(1)产品使用说明书。
(2)产品技术条件(或企业标准),建立技术资料。
(3)产品电器原理图、线路图、方框图。
(4)关键元部件或原材料清单(请选用有欧洲认证标志的产品)。
(5)整机或元部件认证书复印件。
(6)其他需要的资料。
-



